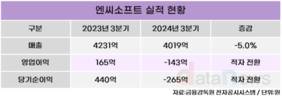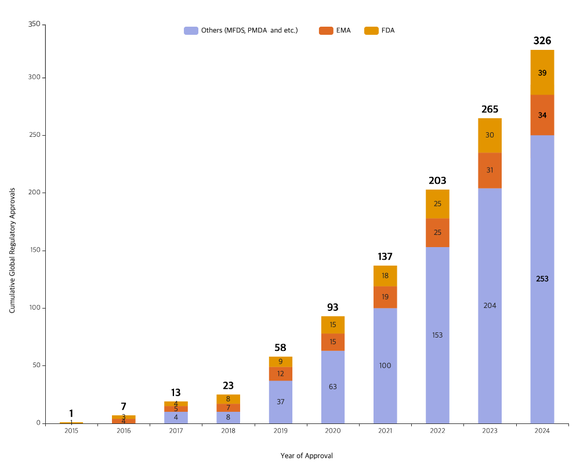
▲제조 품목 글로벌 규제기관 제조 승인 현황 / 자료=삼성바이오로직스
삼성바이오로직스(대표 존림)는 창립 13년 만에 제품 허가 기준 글로벌 규제기관 제조 승인 건수 300건을 돌파했다고 10일 밝혔다.
규제기관 제조 승인은 바이오의약품의 제조 및 관리 전 과정에 대해 약품 제조 및 품질관리기준(GMP) 및 품질 적합성이 검증 됐음을 의미하는 것으로, 위탁생산(CMO) 기업이 생산한 의약품을 시장에 출시하기 위해서는 해당 국가 규제기관의 승인이 필수적이다.
삼성바이오로직스는 9월 기준 미국 식품의약국(FDA) 39건, 유럽 의약품청(EMA) 34건 등 총 326건의 제조 품목 규제기관 제조 승인을 획득했으며, 생산능력 확장 및 수주 증가에 따라 해마다 승인 건수를 늘려가고 있다. 규제기관 실사 통과율은 업계 최고 수준을 유지하고 있다.
삼성바이오로직스가 까다로운 규제기관의 실사에도 성공적인 트랙레코드를 쌓아가며 세계적 수준의 품질 경쟁력을 입증한 배경에는 전문 인력 양성, 전자 데이터 관리 시스템, 비대면 실사 역량 구축 등이 꼽힌다.
존림 삼성바이오로직스 사장은 “글로벌 제약사 제품 수주와 신속한 규제기관 인증 획득을 통해 삼성바이오로직스는 지난 13년 간 CDMO 분야에서 유례없이 빠르게 성장해왔다”며 “앞으로도 품질경영을 기반한 끊임없는 기술 혁신을 통해 고품질의 바이오의약품을 시장에 적기 공급할 수 있도록 최선의 노력을 다하겠다”고 말했다.
한편 삼성바이오로직스는 현재 시가총액 기준 글로벌 톱 20개 제약사 중 16곳을 고객사로 확보하고 있다. 또한 단일 계약 기준 역대 최대 규모인 1조4600억 원 규모의 초대형 계약을 비롯 올해에만 총 8건의 신규 및 증액 계약을 체결하며 연 누적 수주 금액 2조6000억 원을 돌파했다.
성수아 기자 sa358@datanews.co.kr
[ⓒ데이터저널리즘의 중심 데이터뉴스 - 무단전재 & 재배포 금지]
많이 본 뉴스